|
ʮ����������ѧ����һֱ�������˽�colibactin---һ����ijЩ�˾���������Ļ�����---���ֱ����֮��Ĺ������������ܹ��������ֻ������һֱ���衣��ˣ����������ѧ��ѧ�뻯ѧ����ѧ����Emily Balskus������ʰ�����̯�ӡ�
��һ���µ��о��У�Balskus����ͬ������ͼͨ��ȷ�ؼ�����colibactin�����DNA������Ӧ����DNA�Ӻ������������ֻ�������ε��°�֢������о����������2019��2��15�յ�Science�ڿ��ϣ����ı���Ϊ��The human gut bacterial genotoxin colibactin alkylates DNA����
Balskus˵������2006�����������Ǿ���֪��ijЩ��������ϸ��---��Ҫ�Ǵ˾�����---����һ���������ܹ��ϳɵ���DNA���˵ķ��ӵĻ������������������о�����Я�����ֺϳ�;����ϸ���ķ�������֢֮���������ԣ����ҽ᳦����ؽ�ֱ�����Ķ���С��ģ����֤ʵ�������ض��Ļ����ܹ�Ӱ�������Ľ�չ����Ϯ�ԡ���
���ҵ��ǣ���ĿǰΪֹ����ѧ���ǻ�û���ҵ�����ͨ������;��������colibactin�ķ��������ʹ�����Ƕ��������û���һ����֪��
Balskus˵�����ҵ�ʵ���ҿ�ʼ�о���һ�㣬������Ϊ���Ƕ����������������ķ��ӵ��������Ȥ��������ǰ��colibactin�о��Ľ��������Ǻ������о�����;����������������֮��ط���������Ȼ���ﺬ����ν�Ļ����黷��cyclopropane ring������
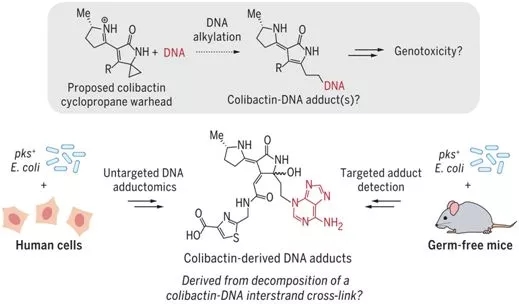
Balskus����ͬ������Ϊ�������ֻ�ѧ�ṹ�γ���colibactin��ͷ��������Ϊ���ƵĽṹ�����������ص��ܹ�ͨ����DNA������Ӧ����DNA���˵ķ����С�
Balskus˵������������ʶ����һ��ʱ�����Dz²���DNA��ֱ������ÿ�����colibactin�Ļ�����������������Ҫ�����á���Ϊ��ȡ�й�colibactin�ṹ����Ϣ�ṩ���µIJ���---���Dz�����ͼ�������ֻ����ﱾ���������ܹ��������������DNA������Ӧ�������DNA�Ӻ����
Ȼ����������ЩDNA�Ӻ��ﲢ�����¡�Ϊ��������һ�㣬Balskus�������Ŷ�Ѱ�����������մ��ѧ��������ѧԺ����Silvia Balbo�İ�����Balbo������һ���µļ��������������ܹ�������ЩDNA�Ӻ����ڸ߷ֱ����������в�������Ƭ���������ǡ�
Balskus˵����������������ʵ����ǻ�ȡһ���ܹ�����colibactin�Ĵ˾������һ�־�����ͬ�����͵Ĵ˾�ͻ����꣬����ͻ������Ψһ��ͬ������û�в���colibactin�Ļ���ء����ǽ������־�������ϸ��ϵһ������......������������ϸ���з����DNA�����������������У����Ƚ���Ʒ�в�ͬDNA�Ӻ���ķ�ȣ��������Ǿ��ܹ����ֽ��ɾ�������colibactin��ϸ�����괦������ϸ��ϵ������DNA�Ӻ����
Balskus˵����������Щ��Ϣ֮�����ǵ���һ����ս��������ЩDNA�Ӻ���Ļ�ѧ�ṹ��Balskus˵���������������в�������Ƭ�����ǿ���������colibactin�������Ⲣ������������Ļ�ѧ�ṹ����ʵ���ҵ��о���Ա�����ģ���һ��Ӣ�µ�Ŭ���������û�ѧ�����ϳ���һ�ֱ�Ʒ����Ȼ�����ǽ���������Щ��ϸ��ϵ�в�����DNA�Ӻ�����бȽϣ�������һ���ġ���
Ϊ��֤ʵ�������Ҳ�ڻ�Ķ������������ã�Balskus�Ŷ������������������������ѧԺ��Wendy Garrett������չһ��ʵ�飬������ʵ���У����ܹ�����colibactin�Ĵ˾�����Ͳ��ܹ��������ֻ�����Ĵ˾����궨ֲ����С�����ڡ�
Balskus˵�������Ƿ��������ڽ����ܹ�����colibactin�Ĵ˾����궨ֲ��С��᳦��Ƥ��֯�м���Щ��ͬ��DNA�Ӻ����������Ǻ���������������е����л�ѧ��Ӧ���������������ڷ����������йء���
չ��δ����Balskusϣ���о������Ƿ��ܹ��ڻ��������м���Щ��ͬ��DNA�Ӻ�����˽�colibactin������ض����͵�DNA�����Լ������Ƿ��Ӱ�착֢������
| 
 ��ѯ���ߣ�
��ѯ���ߣ�
